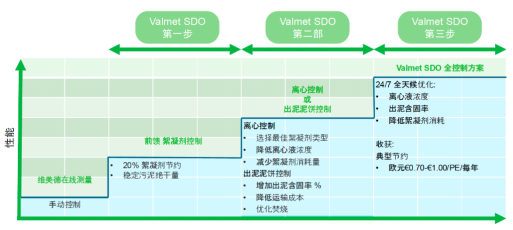
华东理工大学周彦波团队JCLP:铁钴负载氮化碳双金属催化剂活化过硫酸盐降解双酚A
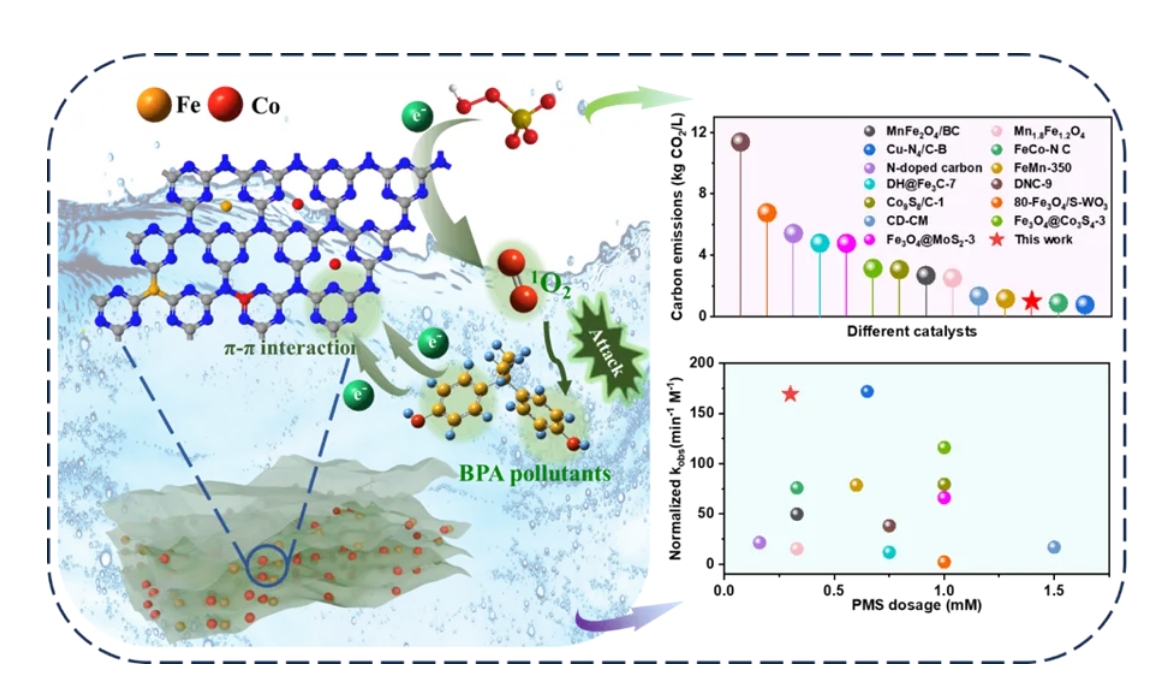
图文摘要
成果简介
本研究采用一步热缩聚法制备了活化过硫酸盐(PMS)催化剂(Fe/Co-CN),用于高效处理含双酚A (BPA)废水。Fe/Co-CN的金属浸出率低(<1 mg/L)大大减轻对环境的潜在风险。同时Fe/Co-CN对BPA有良好的催化降解性能,5 min降解效率为90.7%,10 min降解效率为~100%,远高于单金属负载的Fe-CN (77.2%)和Co-CN (73.2%)。在Fe/Co-CN/PMS体系中,以1O2和高价物种为主的非自由基物种为主要活性氧物种。通过严格控制Fe/Co-CN合成和应用过程中的能量消耗,实现了比报道的大多数催化剂更低的碳排放。Fe/Co-CN合成和应用对于高级氧化技术处理有机微污染物具有重要意义,为催化剂合成过程的碳排放量的计算提供了参考。
引言
目前,新污染物在环境中已不断被检出,即使在低浓度下,仍对生态系统和人体健康有威胁。双酚A是一种典型的新污染物,其对健康的不良影响已得到充分证明。高级氧化工艺(AOP)是一种有前途的工艺,AOP可以生产具有高氧化电位的活性氧(ROS),ROS可以将有机污染物进行降解和矿化,转化成无害的副产物。过硫酸盐(PMS)在AOPs领域发挥着重要作用。在最近的研究中,金属氧化物/硫化物对过硫酸盐有良好的催化性能。然而,金属氧化物/硫化物在活化PMS过程中经常会出现大量金属离子的溶出现象,一方面会形成“均相-非均相”复合催化体系,另一方面金属离子浓度过高也会对人体健康造成威胁,在很大程度上限制了金属基催化剂在实际场景中的应用。与此同时,我们发现多数催化剂合成方式极度复杂,其中包含多重加热环节,在合成的过程中会造成巨大的碳排放。这样的“新催化剂”不符合各国针对减少碳排放所指定的政策。针对上述问题,通过一步热缩聚法合成Fe/Co-CN,使用了极少的金属负载就可以实现高效的污染物降解。同时,Fe/Co-CN/PMS系统有极低的Co和Fe溶出(<1 mg/L),大大降低应用过程中对环境的潜在风险。我们选取代表内分泌干扰物的BPA作为模型污染物,在不同工艺参数、不同水质参数下对Fe/Co-CN进行性能评价。还探究了Fe/Co-CN活化PMS降解BPA的机理。我们进行了连续柱实验证明Fe/Co-CN具有工业应用潜力。
图文导读
Fe/Co-CN采用一步热缩聚法合成,将Fe、Co两种金属成功掺杂进氮化碳骨架中。通过TEM,HRTEM和能量色散光谱(EDS)分析表征了Fe/Co-CN的形态和成分。催化剂仅分布在氮化碳的碳质骨架,且骨架上不含有金属颗粒。

图1(a)Fe/Co–CN 的制备示意图;(b)Fe/Co-CN催化剂TEM和(c)HRTEM图,(d)高分辨图(插图为SEAD选区电子衍射图),(e)HADAF模式下HRTEM图及和对应元素的Mapping图,(f)C,(g)N,(h)O,(i)Fe,(j)Co
无金属负载的C3N4具有最小的催化活性,BPA 降解效率低于 1%。Fe 和 Co 掺杂后,单一金属催化剂的 BPA 降解性能得到显著提高。10 min的降解效率分别为 77.2% 和 73.2%。Fe和 Co(Fe/Co–CN)共掺杂后,在较低的氧化剂投加量(0.3 mM)和较低的催化剂投加量下(0.1 g/L), 5 min 降解效率为 90.7%,10 min 降解效率为 ∼100%。
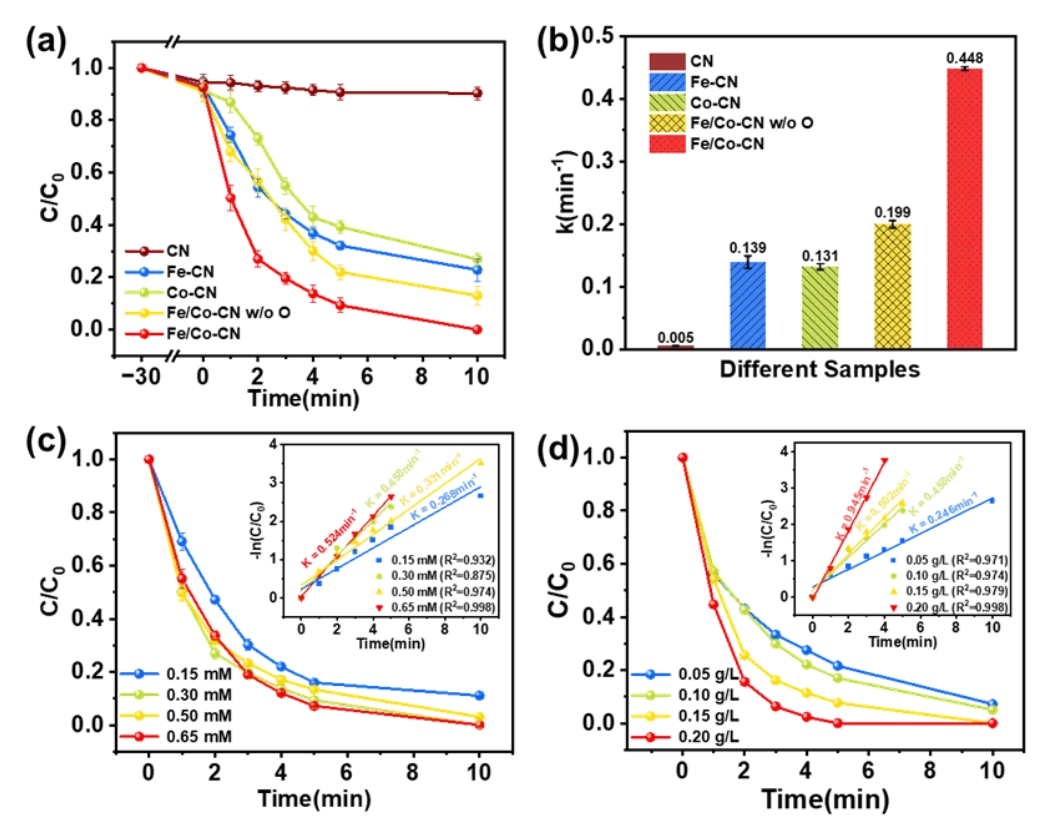
图2 (a) CN、Fe-CN、Co-CN、Fe/Co-CN w/o O和Fe/Co-CN对BPA的降解效率。(b)为(a)的表观动力学常数。(c)不同PMS用量下Fe/Co-CN催化降解BPA的效率及表观动力学常数(插图)。(d)不同催化剂用量下Fe/Co-CN催化降解BPA的效率及表观动力学常数(插图)。
DMPO-SO4·-/·OH呈现出 DMPO-X(1:2:1:2:1:2)的七重峰,而不是SO4·-/·OH自由基的典型信号。这可能归因于单电子氧化途径,不需要·OH或经过深度氧化后即可产生。结合淬灭实验和EPR测试结果,Fe/Co-CN/PMS体系中主导的活性氧物种仍为高价金属和1O2,同时有少量的·OH存在。
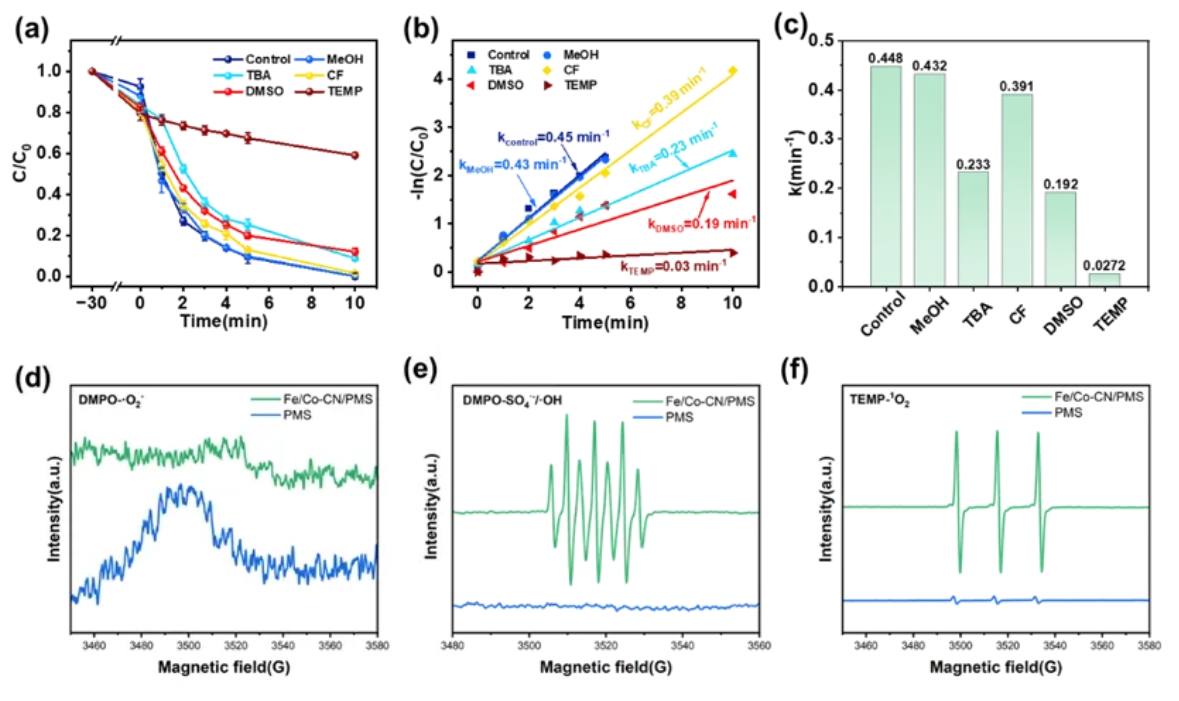
图3 (a)不同猝灭剂对BPA的降解效率的影响,(b)降解动力学,(c)不同猝灭剂下动力学常数比较。不同体系PMS活化的EPR光谱(d)DMPO-O2·-, (e)DMPO-SO4·-/·OH, (f)TEMP-1O2.
通过循环实验和连续柱实验来评估 Fe/Co-CN 的稳定性。5 次循环实验的BPA降解效率分别为∼100%、∼100%、91%、68% 和50%。两种金属离子的浸出量小于 1 mg/L。对循环 1、3 和 5 次的XPS 图谱表明催化剂的整体结构成分没有明显变化。C 1s 光谱强度明显增加。N 1s 和O 1s 的强度趋于升高。推测在降解过程中,大量酚羟基结构聚集在Fe/Co-CN催化剂表面。通过煅烧再生,使得催化剂恢复良好降解性能。同时构建了基于Fe/Co-CN/PMS体系的连续柱实验。Fe/Co-CN/PMS体系在流速为2 mL/min时表现出优异的降解能力。15小时后,出水BPA浓度为初始浓度的10%。这进一步表明Fe/Co-CN在水净化领域具有实际应用潜力。
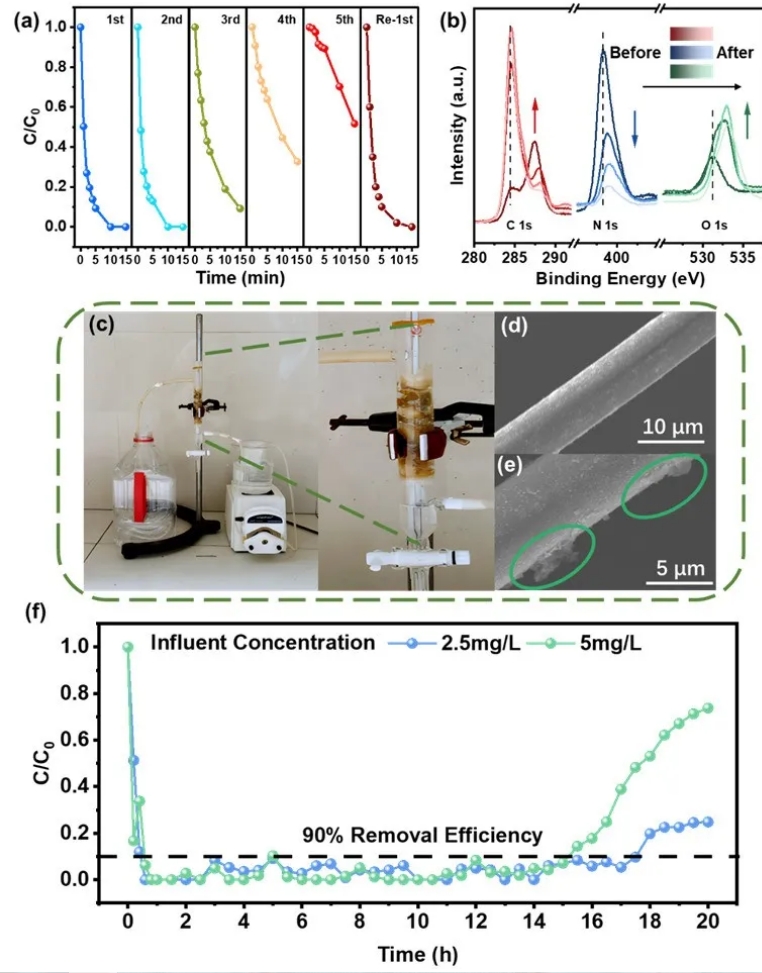
图4.(a)循环实验对Fe/Co-CN催化剂降解性能的影响;(b)反应后催化剂XPS峰强度的变化。(c)模拟连续流柱照片;(d)负载前和(e)负载后棉花的SEM图像;(f)两种不同BPA浓度下的去除效率
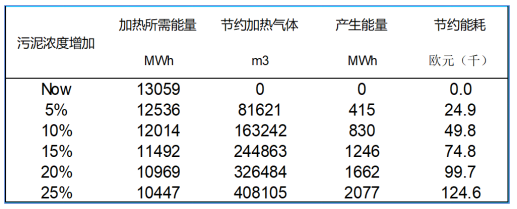
材料合成分为合成、清洗和干燥三个部分。我们根据合成过程中设备的使用情况粗略计算出合成过程所消耗的电能(式(1)、(2))。根据生态环境部报告,中国电网2022年平均排放因子为0.5703吨CO2/Mwh,取0.5703 kg CO2/kwh作为后续电能转换的碳排放系数(式(3))。通过调整原料用量,可模拟单次合成过程生产1 g催化剂,以文中最优催化剂用量为基础,计算处理1L污染物浓度为10 mg/L的废水时,不同催化剂所消耗的催化剂量。式(3)计算合成1g催化剂产生的碳排放量,由此可计算出处理1L浓度为10mg/L的废水的碳排放量(式(4))。经过计算,Fe/Co-CN处理1L污染物浓度为10 mg/L的废水的碳排放量低于多数已报道催化剂。

PC(x)为合成/洗涤/干燥过程的耗电量,单位为kwh。EP为设备功率,单位为kw。T为设备使用时间,单位为h。PC(Total)为合成过程总耗电量,单位为kwh。PC(synthesis)/PC(washing)/PC(drying)为合成/洗涤/干燥过程的耗电量,单位为kwh。CE为耗电量产生的碳排放量,单位为kg CO2。CE-10为处理1L浓度为10 mg/L的废水的碳排放量,单位为kg CO2/L。CD为处理1L废水所消耗的催化剂用量,单位为g/L。
小结
本工作通过简单的一步热缩聚反应合成了Fe、Co负载氮化碳的高效催化剂(Fe/Co–CN)。Fe/Co–CN合成工艺简单,合成过程碳排放较低。通过原位双金属掺杂和氧掺杂,破坏局部电子结构,提高了催化活性。低催化剂用量(0.1 g/L)和低PMS用量(0.3 mM)即可实现BPA高效降解(∼100%),高于单金属负载的Fe-CN(77.2%)和Co-CN(73.2%)。结合猝灭和电化学实验,探究了Fe/Co–CN活化的PMS降解BPA的机理,非自由基体系为主导途径(1O2和高价态物种)。在3.2至10.9的初始pH范围内表现出对BPA高效降解。通过连续流动柱实验验证了Fe/Co-CN/PMS体系的工程应用潜力。总之,本工作为高级氧化工艺处理环境污染提供了理论支持和技术手段。