如何降低饮用水中亚硝胺类副产物生成风险
以经过常规工艺处理的水厂出水为试验用水,借助GC-MS/MS对主体水、模拟管网水以及实际管网水中亚硝胺类消毒副产物含量进行了测定分析,得到了主体水与管网水中亚硝胺含量变动特征,分析了管网对消毒副产物迁移转化的影响作用。
引用本文:马凯,胡艳伟,柴萍. 饮用水中亚硝胺类消毒副产物含量变化特征研究[J]. 给水排水,2023,49(9):12-19.
01试验材料与方法
1.1 试验装置
本研究分别对主体水、模拟管网水、实际管网水中亚硝胺含量变动特征进行了研究。其中,主体水试验采用17 L的聚碳酸酯蓝色透明水桶,同时为避免紫外线照射影响,在水桶外侧做遮光处理。模拟管网试验采用管道反应中试装置,该装置主要由水箱(约300 L)、搅拌器、集成控制箱、3台不同流量范围的水泵及对应浮子流量计、目标试验管道以及不锈钢支架和阀门等部分构成,借助3台水泵可实现循环流量在0~12 m3/h内任意调节,目标试验管道是从实际管网中截取的6段相同铸铁管道(长度1m,管径100 mm),采用串联的方式安装于系统之上,试验装置及组成情况见图1。

图1 管道反应中试装置
1.2 试验方法与样品采集
在主体水试验中(记为M1),以2020年2月天津市某净水厂出厂水(余氯1.1~1.2 mg/L,pH 7.8~8.0,浑浊度0.1~0.15 NTU)作为试验用水,装于聚碳酸酯水桶内,此时作为试验零时刻,随后分别于0.5、1、4 h采集水样,进行亚硝胺类副产物浓度测定。
在模拟管网试验中(记为P1),采集与试验M1同批次出厂水作为试验用水,向中试装置中注入约300 L试验用水,此时作为试验零时刻,在低流速下(0.081 m/s)运行试验装置。随后,分别于0.5、1、2、4 h采集水样,进行亚硝胺类副产物浓度测定,用于比较在相同水源、相近水温条件下,主体水与管网水中亚硝胺含量变动行为差异。此外,为了讨论消毒剂组成调整后管网水亚硝胺含量差异,于2020年6月对自由氯维护消毒(取消现有工艺中硫酸铵投加)与投加氨水(代替现有工艺中硫酸铵)两种余氯衰减控制措施开展模拟管网试验(分别记为P2、P3),分别于0、24、48、72 h采集水样,进行亚硝胺类副产物浓度测定。特别地,在试验P3中,于48 h另采集一份水样,置于玻璃烧杯内,进行煮沸处理,待水温自然冷却至室温后,封装留待测定,用于分析煮沸处理对亚硝胺类物质的去除作用。在试验P2中,于自由氯维护消毒阶段(转为氯胺消毒开始前24 h)采集一份水样,封装留待测定,用于比较自由氯消毒与氯胺消毒阶段亚硝胺含量差异。
针对实际管网水,于2020年6月份采集两座目标水厂及对应两条输水路径(分别记为R1、R2)上的8个监测点水样,进行亚硝胺类副产物浓度测定。
给水系统中亚硝胺含量为ng/L级别,为此每个水样采集量为5~6 L,通过后期的浓缩处理,提高测试样品中待测物含量。由于高密度聚乙烯(HDPE)材料不含有仲胺、叔胺、季胺等易于产生亚硝胺的有机官能团,同时具有很高的化学惰性,因此采集的样品用HDPE水桶进行临时性盛放,并分批送至检测机构进行后处理与测试工作。
1.3 测试方法
1.3.1 亚硝胺类物质萃取
在上机测定亚硝胺类物质前需先后进行过滤处理、固相萃取处理,本研究所采用的固相萃取柱为椰壳活性炭柱。萃取方法主要分为4个步骤:
(1)活化。水样前处理前需对椰壳活性炭柱进行活化处理,本研究依次采用6 mL二氯甲烷、12 mL甲醇、15 mL超纯水对椰壳活性炭柱进行活化,活化后停留5 min上样。
(2)进样。进样前先用甲醇对进样器进行润洗,润洗后将进样器放入样品瓶中进样,在进样过程中保持流速不超过5 mL/min。
(3)洗脱。进样结束后,用氮气将萃取柱吹干防止水分残留影响结果,吹干后用12 mL二氯甲烷洗脱椰壳活性炭柱,收集洗脱液。
(4)浓缩。用氮吹仪在40 ℃下对洗脱液进行氮吹,将洗脱液浓缩至0.5 mL,再用二氯甲烷定容至1 mL,转移至气相小瓶中,加入内标混匀,随后进行GC-MS/MS检测。
1.3.2 亚硝胺类物质测定
亚硝胺类物质含量采用GC-MS/MS测定。
(1)标准溶液配制。9种亚硝胺类物质标准品的浓度为2 000 mg/L,以色谱纯二氯甲烷配制亚硝胺类物质中间使用液质量浓度为1 mg/L,内标中间使用液浓度为100 μg/L。将亚硝胺类物质中间使用液加于进样小瓶中,用色谱纯二氯甲烷逐级稀释为1、5、10、20、50、100、200 μg/L,并分别加入100 μL内标物中间使用液,使得亚硝胺类物质标准溶液中内标物的浓度为10 μg/L。
(2)仪器参数。气相色谱分析条件:VF-1701色谱柱(30 m×0.25 mm×0.25 μm),进样口温度280 ℃,进样方式为不分流进样(1 min),载气为高纯氮气;柱温程序:40 ℃保持2 min,以5 ℃/min速率升温至100 ℃并保持3 min,再以25 ℃/min速率升温至240 ℃保持3 min,再以50 ℃/min速率升温至280 ℃保持5 min;进样体积为2 μL。
串联质谱分析条件:离子源为EI电离源;离子化能量为70 eV;离子源温度为230 ℃;传输线温度为280 ℃;溶剂延迟设置时间为5 min;数据采集方式为多级反应监测(MRM)模式。9种亚硝胺类物质及内标物的质谱参数根据文献和实际色谱柱改良后见表1,亚硝胺类物质的色谱图见图2。
表1 9种亚硝胺类物质的质谱测试条件


图2 含有9种亚硝胺类物质及内标物的标准溶液的MRM色谱图
(3)标准曲线建立。本研究采用内标法建立标准曲线,以9种亚硝胺类物质的浓度作为横坐标,以9种亚硝胺类物质与两种内标物质(NDMA-d6、NDPA-d14)的相关响应为纵坐标,绘制标准曲线,曲线的拟合优度R2在0.9913~0.9996。
1.3.3 其他水质参数测定
试验过程中对水温、总余氯浓度、浑浊度进行监测。其中,浑浊度以浑浊度仪(TU5200,哈希)测定系统出水浑浊度,总余氯值以N,N-二乙基对苯二胺(DPD)法,采用便携式余氯仪(DR300,哈希)测定,水温采用便携式温度计测定。
02结果与讨论
2.1 主体水中亚硝胺含量变动特征
饮用水中亚硝胺含量与原水、处理工艺等因素直接相关。图3展示了冬季与夏季出厂水中9种亚硝胺类副产物的组成情况。由图3a可知,冬季经过常规处理工艺净化后的出厂水中9种亚硝胺均有检出,除NMOR外其他8种亚硝胺含量均超过1 ng/L。对比美国环保局(US EPA)公布的各种亚硝胺的限值,发现NDMA与NDEA含量非常接近限值。进一步,分析夏季出厂水中亚硝胺赋存情况(见图3b),可知NDMA与NDEA含量大幅增加,增幅分别为590%和850%,均超过限值,即终身饮用该水体会有超过10-5的风险罹患癌症,但是NDMA含量远低于我国新出台的国标《生活饮用水卫生标准》(GB 5749-2022)中规定的NDMA限值(100 ng/L),整体上出厂水因NDMA含量超标致病风险较低。另一方面,其他7种亚硝胺含量较冬季出水表现出显著下降。这说明季节变化会导致出厂水中亚硝胺相对含量产生显著变化,这可能是由夏季高藻期原水中有机物组成发生改变所引起的。整体上,由于冬季和夏季出厂水中NDMA与NDEA含量均较高,同时考虑到两种物质的强致癌性,因此接下来仅对以上两种亚硝胺类副产物进行重点分析。
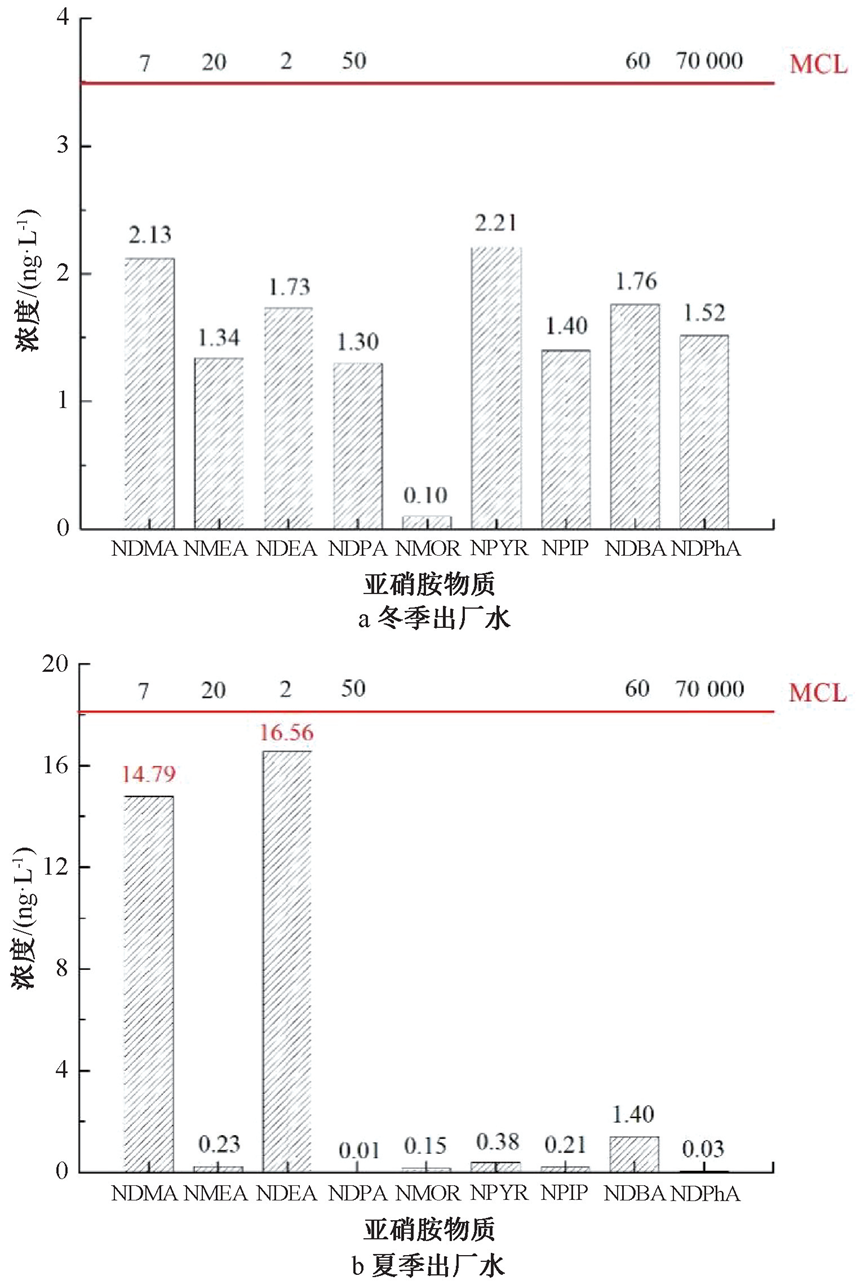
注:红线以上数值(MCL)对应各种亚硝胺致癌风险为10-5时的最大允许浓度
图3 出厂水中9种亚硝胺类消毒副产物含量
为了表明原水化学特性对亚硝胺生成的影响作用,本研究同时对以超纯水配制的氯胺溶液进行GC-MS/MS表征,9种亚硝胺相对含量如图4所示。比较可知,储备液中7种亚硝胺含量均极低(<0.1 ng/L),NDMA含量为0.32 ng/L,而NDEA含量超过图中限值,达到2.89 ng/L。这说明即使在超纯水中,也存在生成亚硝胺的前体物质,在遇到氯胺消毒剂时,会生成亚硝胺类消毒副产物。
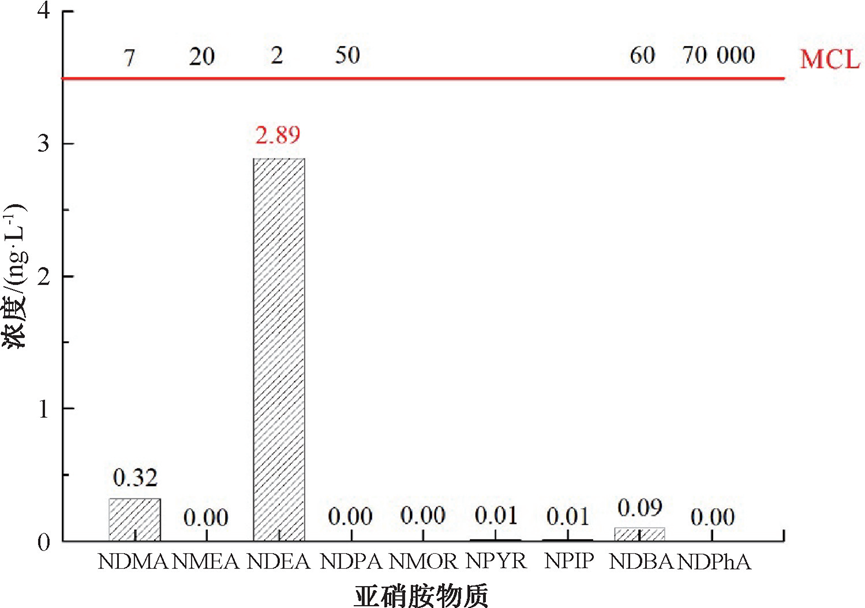
图4 以超纯水配制的氯胺储备液中9种亚硝胺类副产物含量
试验中所使用的Millipore超纯水机采用了离子交换-紫外照射-超滤处理工艺,其中离子交换工艺所采用的阴离子交换树脂是由含有季铵盐官能团的交联聚合物组成。有研究证实,季铵盐是生成亚硝胺的一类重要前体物质,甚至可导致处理后的水中NDMA含量高达223 ng/L。因此,推断是由于离子交换树脂的存在导致了超纯水中含有痕量的前体物,在遇到氯胺消毒剂后生成了NDMA与NDEA。因此,在开展饮用水中亚硝胺类消毒副产物研究中,应谨慎使用经离子交换法净化后的实验用水,避免对试验结果产生干扰。
图5展示了主体水试验(M1)中NDMA与NDEA含量随时间变动情况。观察可知,经过净化处理的出厂水中含有一定量的NDMA与NDEA,两种亚硝胺含量之和表现为先降低,再升高,随后再降低的变化趋势,这主要是由NDEA含量出现大幅波动所导致的。反观NDMA,其含量表现为随时间延长而逐渐降低的变动特征。
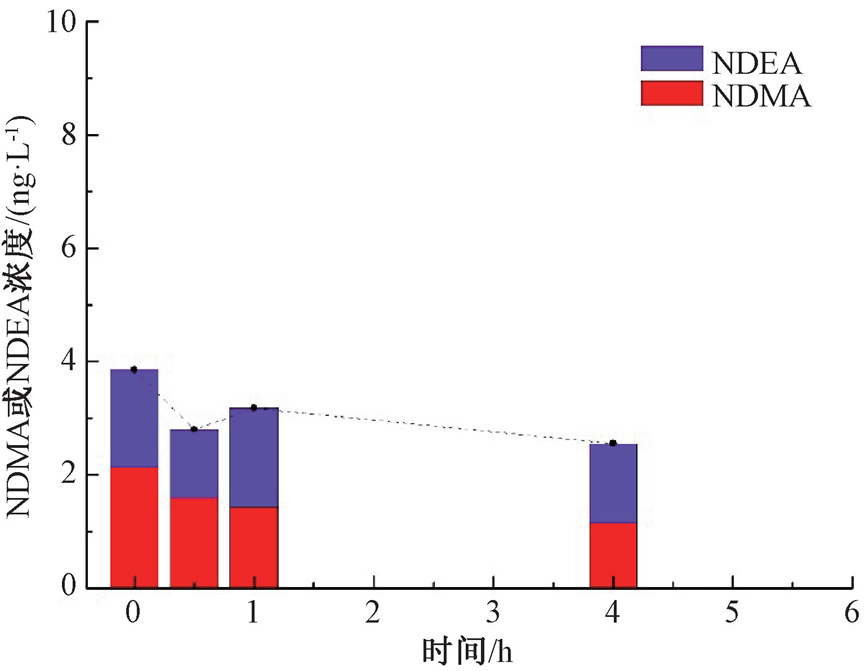
图5 主体水实验中NDMA与NDEA含量随时间变动情况
研究发现,亚硝胺中N-N共价键能较低,因而在热解过程中优先断裂。另有一项机理研究发现,亚硝基吡咯烷(NPYR)在光解过程中,首先断裂N-N共价键,生成吡咯烷与NO-2或NO-3,吡咯烷进一步发生开环反应,断开C3—C4间共价键,生成二乙基胺,NPYR降解途径如图6所示。比较分析主体水试验中NDEA与NPYR含量变动情况,可知NPYR含量自初始2.21 ng/L逐渐降低,至0.5 h下降至1.16 ng/L,特别在0.5~1 h期间,浓度降低了0.49 ng/L,同期NDEA浓度升高了0.54 ng/L。由此推断,水中NPYR发生了开环反应生成NDEA,是导致NDEA含量升高的原因。
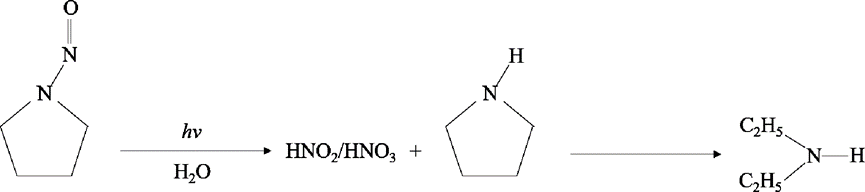
图6 推断的NPYR降解途径
2.2 管网水中亚硝胺含量变动特征
首先,对不同条件下模拟管网水中亚硝胺含量变动特征进行分析。图7展示了冬季模拟管网水中NDMA与NDEA含量随时间变动情况。观察可知,NDMA与NDEA两种亚硝胺含量在0~0.5 h期间均表现出先升高,随后逐渐降低的特征。这与相同条件下主体水试验结果有所不同,主要表现在初始阶段NDMA含量的小幅升高方面,分析是由于中试装置中存在大量的微生物及其代谢产物,在接触氯胺消毒剂后生成亚硝胺类消毒副产物所致。另外,其他7种亚硝胺中仍有5种亚硝胺在0~0.5 h期间表现出升高的变动特征,这也表明需要对微生物滋生所引发的亚硝胺污染进行重视。
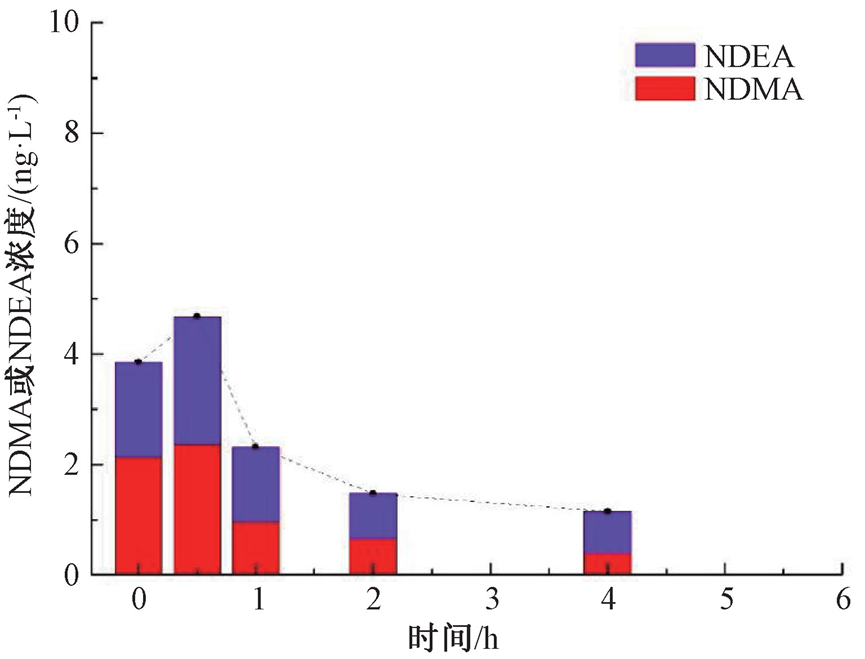
图7 模拟管网水氯胺衰减实验中NDMA与NDEA含量随时间变动情况
另一方面,比较分析管网水试验中NDEA与NPYR含量变动情况,可知在0~0.5 h,NPYR浓度降低了0.58 ng/L,同期NDEA浓度升高了0.59 ng/L,这种截然相反的浓度变动特征进一步证实水中NPYR可转化为NDEA。
有研究表明,对氯胺消毒管网周期性采用自由氯消毒,能够有效抑制管道微生物滋生,取得良好的消毒效果。为此,对自由氯消毒期间与切换为氯胺消毒后模拟管网水中亚硝胺含量的变动规律进行分析。图8展示了自由氯消毒阶段与切换为氯胺消毒后模拟管网中NDMA与NDEA含量随时间变动情况。观察可知,在氯胺消毒阶段(图8中虚线右侧部分),NDMA与NDEA含量在0至48 h期间逐渐降低,而两者含量在72 h较48 h分别增加了2.57、0.36 ng/L,
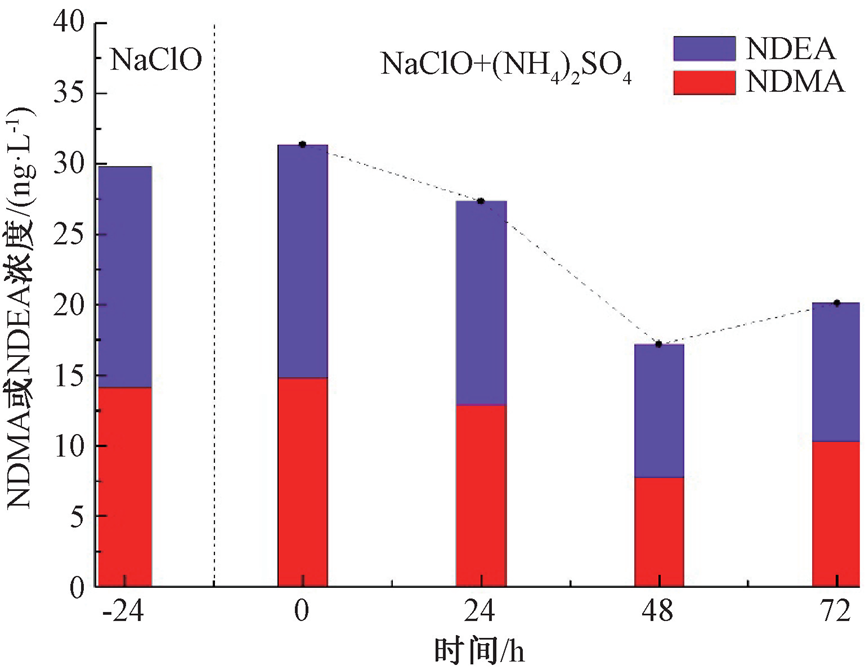
图8 试验P2中NDMA与NDEA含量随时间变动情况
不仅如此,NMOR、NDPA、NPIP也表现出了反弹升高的变动趋势。在自由氯维护消毒措施研究中(试验P2),试验开始后8 h出水余氯浓度已低于0.20 mg/L,较低的氯胺浓度不利于亚硝胺类物质的生成。LIU等、KRANSER等研究发现,微生物代谢产生溶解态有机物可作为活性前体物生成消毒副产物。有研究发现,给水管网中氯胺与有机物接触时间越长,亚硝胺类副产物生成量越高。因此,推测试验后期亚硝胺含量的显著增加是由微生物代谢产生大量亚硝胺生成前体物,遇到低剂量氯胺后生成亚硝胺所导致的。
在试验P2中,同样对自由氯消毒阶段的出水亚硝胺浓度进行了测定(图8中虚线左侧部分)。比较可知,在自由氯消毒阶段,试验出水中NDMA与NDEA含量与同期出厂水基本持平,甚至高于氯胺消毒阶段中24、48、72 h出水含量。这表明将氯胺消毒系统更换为自由氯消毒后同样存在亚硝胺类副产物生成风险,其中活跃的微生物代谢作用可能为亚硝胺生成提供了必要的胺类前体物。因此,无论从消毒剂衰减控制角度,还是从亚硝胺生成控制角度,均应对管道微生物污染问题给予足够的重视。
图9展示了投加氨水试验中NDMA与NDEA含量随时间变动情况。由图9可知,在连续监测过程中NDMA含量不断下降,NDEA含量表现为先降低,在72 h再度升高的变动特征,这与自由氯维护消毒实验结果相同。这也进一步证实微生物代谢水平增加会引起亚硝胺含量升高。在本试验中,特别对48 h出水做煮沸处理,并测定其亚硝胺浓度,结果见图9中粉色和蓝色标识柱。比较可知,经过煮沸处理,NDMA与NDEA含量均呈现下降趋势,下降幅度分别为36.5%与3.8%,同时其他7种亚硝胺含量也不同程度呈现下降趋势,说明煮沸处理对水中亚硝胺,特别是NDMA,具有一定去除作用。
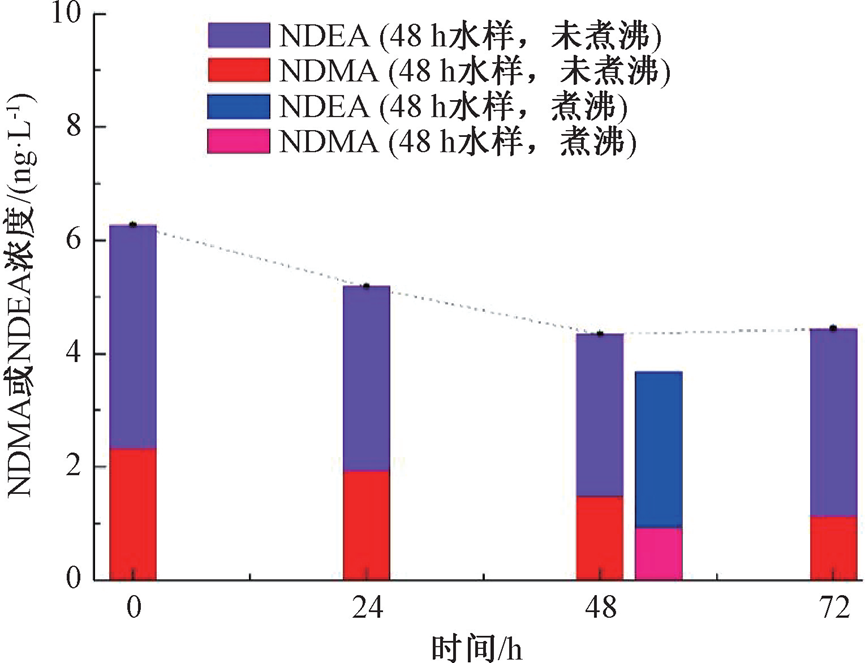
图9 试验P3中NDMA与NDEA含量随时间变动情况
最后,对实际管网中亚硝胺含量的沿程变动规律进行分析。图10展示了R1与R2两条输水路径下NDMA与NDEA含量随水龄变动情况,图中横坐标为各监测点对应水龄。首先,对于供水路径R1,出厂水中亚硝胺含量相对较高,NDMA与NDEA含量分别为35.50 ng/L与21.71 ng/L,在经过4 h输送后,龙头出水中NDMA与NDEA含量大幅下降,这与主体水试验结果相同。在接下来的两个取样点之间,两种亚硝胺含量基本持平,而经过最后的长距离输送,龙头出水中NDMA与NDEA含量再次上升,其中NDMA含量甚至超过出厂水浓度,达到41.31 ng/L。分析远距离管网点出水亚硝胺含量升高的原因是,在夏季下游管道微生物代谢活性较上游显著更强,从而在下游管道中形成更高含量的亚硝胺生成前体物,在接触氯胺消毒剂后即生成亚硝胺类副产物,这与模拟试验中的研究结果相一致。
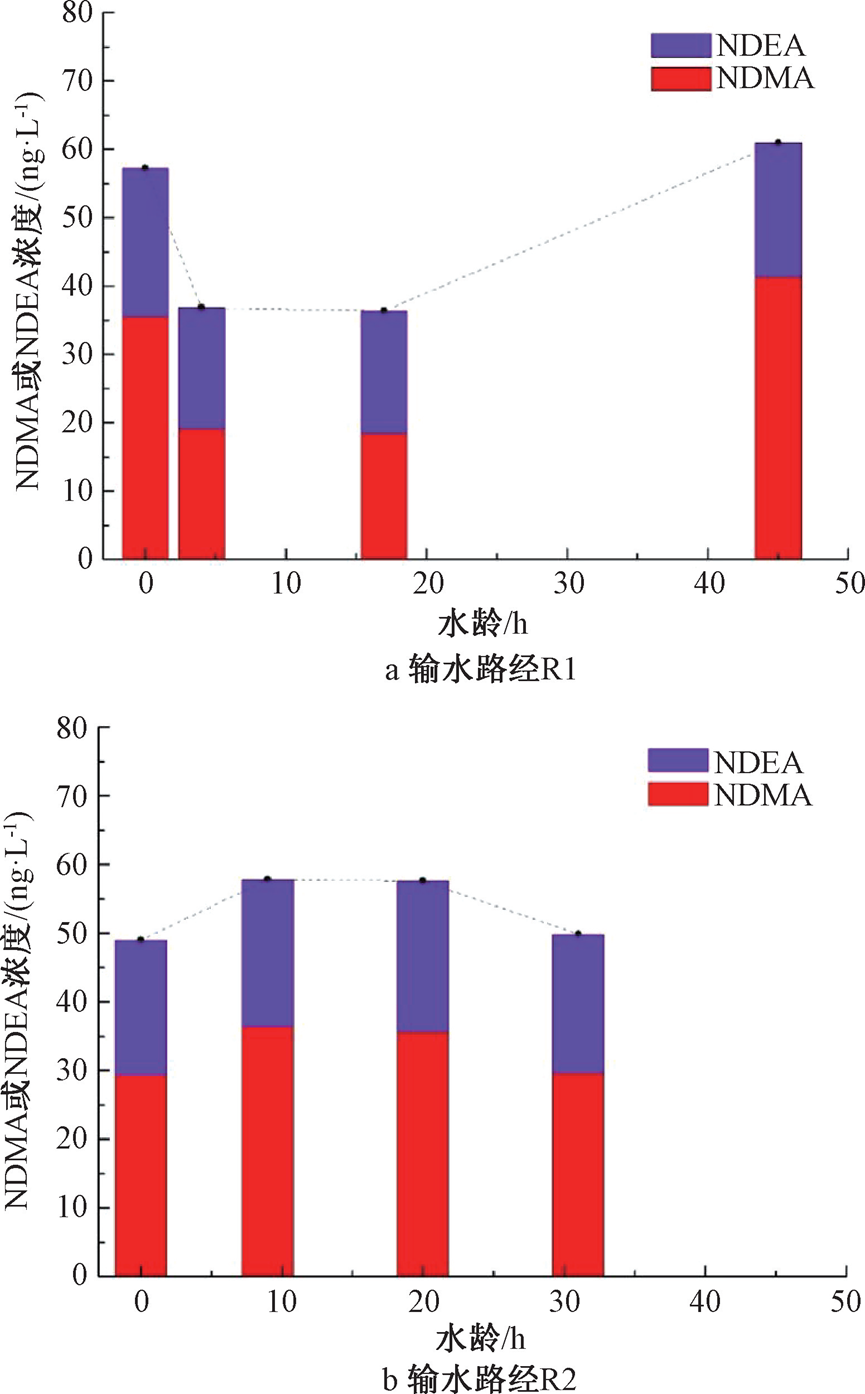
图10 两条输水路径中NDMA与NDEA含量随水龄变动情况
对于供水路径R2,其出厂水NDMA与NDEA含量较另一座水厂(R1)出水更低,分别为29.37 ng/L与19.61 ng/L,且除NDBA外的其他6种亚硝胺含量也表现更低。考虑到两座水厂采用相同水源(南水北调中线工程原水),推测水厂处理工艺的差异是导致出厂水中亚硝胺含量显著不同的根本原因。未来,针对滦河原水供应,需要对相应水处理工艺下的亚硝胺生成特征进行研究,对水源更换下的污染物生成风险进行全面评估。
进一步分析亚硝胺含量沿R2路径的变动特征如图10所示。观察图10b可知,经过9 h输送后,龙头出水中NDMA与NDEA含量较出厂水呈现小幅增长,而在水龄20 h取样点,其龙头出水中亚硝胺含量与9 h取样点基本持平,到第31 h取样点,其龙头出水中亚硝胺含量再次下降。这与R1路径的消毒副产物变动特征截然不同,推测与管道微生物群落结构与代谢活动差异密切相关。无论如何,有效抑制微生物代谢活性不仅能够降低管网中微生物腐蚀与耗氯作用强度,同时能够降低亚硝胺类消毒副产物的生成风险,在今后供水系统运行管理中应作为重点管控目标。
03结论与展望
本研究借助GC-MS/MS对主体水、模拟管网水以及实际管网水中亚硝胺类消毒副产物含量进行了测定分析,得到了主体水与管网水中亚硝胺含量变动特征,具体结论如下:
(1)以丹江口水库水为原水,经过常规处理工艺净化后的出厂水以亚硝基二甲胺(NDMA)与亚硝基二乙胺(NDEA)为主要亚硝胺类副产物,且出厂水中亚硝胺含量存在显著的季节性变动特征,表现为夏季出水中NDMA与NDEA含量显著高于冬季的特征。
(2)在自由氯维护消毒阶段,管道中同样会产生高含量的亚硝胺,因此将氯胺消毒系统更换为自由氯消毒后同样存在亚硝胺类副产物生成风险,切换为氯胺消毒剂后,出水中NDMA与NDEA含量呈现出先降低,最后小幅升高的变动特征。在投加氨水试验中,NDMA含量在试验期内不断下降,NDEA含量表现为先降低,最后小幅升高的变动特征。两项模拟管网试验中出现的亚硝胺含量升高现象,是管道微生物滋生并释放大量亚硝胺生成前体物所导致的。
(3)在实际管网中,沿程NDMA与NDEA含量变动趋势与各区段微生物代谢强度直接相关。因此,抑制微生物代谢活性是降低亚硝胺类消毒副产物生成风险的有效措施。
合理的消毒工艺是保障饮用水水质安全的重要前提。在未来运行管理中,应重点关注下游管网的微生物生长代谢活性,建议开展主动式管道清洗、老旧管网改造工程,同时调整消毒剂组成,降低含氯消毒剂一次投加浓度并应用中途加氯等技术手段,降低亚硝胺类副产物生成风险,提高饮用水安全水平。